Voll kompatibel ? 1) – Zur Praxis von Kompatibilitässtudien an Infusions-, Perfusions- und Injektionslösungen
Von Ulrike Steiner und Wolfgang Woiwode
Key Words: Subvisible Particles, Light Blockage, Visible Particles, Compatibiliy, Leachables and Extractables
Schlüsselwörter: Kompatibilitätsstudie, Infusionslösungen, Injektabilia, nichtsichtbare Partikel, Laserlichtblockade, sichtbare Partikel, Methodenvalidierung, mobile und extrahierbare Stoffe und Komponenten
Ein Meilenstein in der Entwicklung von Injektabilia und Lyophilisaten zur Herstellung von Infusionslösungen ist die Prüfung der Kompatibilität von Wirkstoffen und Hilfsstoffen in den jeweiligen Trägerlösungen und Primärpackmitteln. Das Zusammentreffen von Wirkstoff, Trägerlösung und Primärpackmittel kann zu chemischen und physikalischen Veränderungen direkt in der Zubereitung, wie auch in der Zubereitung im Kontakt mit der Primärverpackung führen. Dabei wirken möglicherweise auch noch Leachables & Extractables (mobile und extrahierbare Stoffe und Komponenten) mit. Letzteres kann in der diesbezüglichen, vorausgehenden Prüfung der Primärpackmittel allein schon der Vielzahl der Kombinationen von Wirkstoffen, Hilfsstoffen, Lösungsmitteln und Lösungsvermittlern wegen nicht vollumfänglich abgehandelt werden kann. Umso zentraler ist daher das Design der Kompatibilitätsprüfung hinsichtlich der Auswahl der Primärbehältnisse, Zwischenbehältnisse und Geräte, der Handhabung der Proben, der Exposition nach Art und Dauer, der Analysenverfahren und des Zeitrahmens, um ökonomisch vertretbar eine gesicherte Aussage zur Kompatibilität treffen zu können.
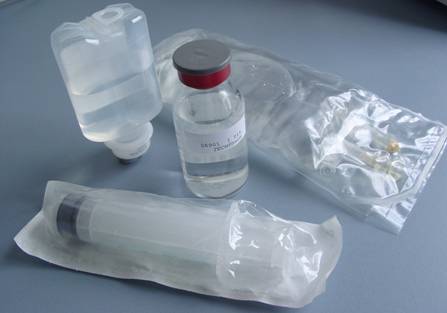
Mögliche Veränderungen der hergestellten Ansatzlösungen können folgende Parameter betreffen: Klarheit, Färbung, pH-Wert, Partikelgehalt nach Art und Größe, Gehalt des Wirkstoffes und Verunreinigungen.
Verminderung der Klarheit nach Ph. Eur. 2.2.1 und die Änderung, meist Zunahme der Färbung nach Ph. Eur. 2.2.2 lassen sich durch Vergleichsmessungen mit Opaleszenzstandards und Farbvergleichslösungen erfassen. Die Quantifizierung einer Trübung kann instrumentell mittels Nephelometrie nach Ph. Eur. 2.2.1 erfolgen. Die Bildung unlöslicher Bestandteile kann graduell zu Trübungen der Ansatzlösung führen und zur Bildung von partikulären Bestandteilen, die dann ab einer Größe von 2 µm mittels Laserlichtblockade nach Ph. Eur 2.9.19 als nichtsichtbare Partikel detektiert werden können und schließlich ab etwa 50 µm zu sichtbaren Partikeln nach Ph. Eur. 2.9.20 wachsen, oder agglomerieren. Eine Abnahme des Gehaltes des Wirkstoffes auch in Kombination mit einer Zunahme von bekannten und unbekannten Verunreinigung kann mittels HPLC nach Ph. Eur. 2.2.29 erfasst werden. Änderungen des pH-Wertes, die ihrerseits einen Einfluss auf die Stabilität des Wirkstoffes und der Zubereitung haben können, können nach Ph. Eur. 2.2.3 verfolgt werden.
Die oben genannten Veränderungen stellen nach Art und Umfang bereits schon mögliche Ausschlusskriterien für eine Kompatibilität dar. Das Design der Studie sollte realistische Bedingungen vorgeben, gleichzeitig aber durch überlegte Handhabung der Proben so weit als möglich Faktoren minimieren, die die beschriebenen Phänomene verstärken oder erst auslösen könnten. Beispielhaft sind im Folgenden unsere Überlegungen und Erfahrungen zu den Parametern Partikel sowie Gehalt und Reinheit dargestellt.
Beispiel sichtbare und nichtsichtbare Partikel
- Vermeidung des Eintrags von Partikeln: die Herstellung der Ansätze sowie die Entnahme von Teilmengen für die Prüfung sollte grundsätzlich in einer Laminar-Flow-Einheit vorgenommen werden. Die dabei verwendeten Hilfsmittel müssen mit bekannten Blindwerten partikelarm bereitgestellt werden.
- Vermeidung von Luftblasen: diese werden als Artefakte als nichtsichtbare Partikel bei der Bestimmung nach Ph. Eur. 2.9.19 detektiert. Als kritischer Punkt sind hier die Art und Weise der Rekonstitution von Lyophilisaten sowie die Überführung der Injektabilia bzw. rekonstituierten Lyophilisate in die Behältnisse mit den Trägerlösungen zu nennen, die laminar oder turbulent erfolgen kann.
- Auswahl der geeigneten Prüfmethode: das Verfahren zur Bestimmung der nichtsichtbaren Partikel nach Ph. Eur. 2.9.19 ist zweistufig und sieht zunächst den Einsatz des Verfahrens Laserlichtblockade vor. Wenn mit diesem Verfahren eine direkte Messung nicht möglich ist, ist das lichtmikroskopische Verfahren anzuwenden. Dieses ist z.B. dann die Methode der Wahl, wenn Luft- oder Gasblasen so wie in Ph. Eur. 2.9.19 angeführt, beim Ansaugen der Ansatzlösung in den Sensor gebildet werden.
- Planung der Abfolge der Prüfungen: Zuerst sollte die Prüfung auf sichtbare Partikel vorgenommen werden, idealerweise im Primärbehältnis, soweit dieses transparent ist, danach die Prüfung auf nichtsichtbare Partikel, danach die weiteren chemischen und physikalischen Prüfungen.
Beispiel Gehalt und Reinheit
Die Stabilität einiger Zubereitungen kann wie im Fall von Proteinen mit zunehmender Verdünnung abnehmen. Im Fall von Kompatibilitätsstudien sind daher gerade hinsichtlich Gehalt und Reinheit zusätzliche Verdünnungsschritte und der zeitliche Ablauf sorgfältig zu planen:
- Durch das Einbringen der wirkstoffhaltigen Zubereitung bzw. der Lyophilisate in die Trägerlösung resultiert eine weitere Verdünnung des Wirkstoffes. Der Grad der Verdünnung hängt davon ab, ob vor Zugabe der wirkstoffhaltigen Zubereitung das gleiche Volumen an Trägerlösung aus dem Gebinde entnommen wird, oder ob eine direkte Zugabe erfolgt. Letztere, die additive Zugabe, entspricht eher der Praxis, führt aber zu einer höheren Verdünnung des Wirkstoffs und ist zudem durch das maximale Zuspritzvolumen des vorliegenden Gebindes limitiert.
- Erfahrungsgemäß sind die Gebinde der Trägerlösungen zur Sicherstellung des entnehmbaren Volumens herstellerseitig überfüllt. Dadurch kann bei Zugabe des Wirkstoffes eine höhere Verdünnung resultieren, als durch das Studiendesign vorgesehen. Als Lösung im Rahmen der Kompatibilitätsstudie kann das intakte Gebinde der Trägerlösung vor Beginn der Studie sowie das entleerte und getrocknete Gebinde nach Abschluss der Studie ausgewogen und in Kenntnis der Dichte der Trägerlösung das tatsächliche Volumen des Gebindes zu ermittelt werden. In gleicher Weise können die Gebinde von Lyophilisaten ausgewogen werden, um Kenntnis der tatsächlich eingesetzten Wirkstoffmenge zu erhalten. Diese Vorgehensweise dient der Sicherstellung der quantitativen Auswertung, ist jedoch nicht relevant für die Art der Anwendung.
- Es ist zu prüfen, ob die im Rahmen der Kompatibilitässtudie zum Einsatz kommenden Methoden zur Bestimmung des Gehaltes und Verunreinigungen für den Konzentrationsbereich des Wirkstoffs in der Ansatzlösung und die Art der Trägerlösung valide sind. Gegebenenfalls sind auch Anpassungen von Geräte-parametern wie z.B. ein höheres Injektionsvolumen bei HPLC-Bestimmungen erforderlich. Gegebenenfalls ist vor dem Start der Studie eine Revalidierung der Methoden zur Bestimmung des Gehaltes und der Verunreinigungen für den vorgesehenen Konzentrationsbereich erforderlich. Dies betrifft insbesondere die Bestimmungsgrenze, die Präzision und die Linearität.
- Die zu den jeweiligen Prüfzeitpunkten entnommenen Teilmengen sind zeitnah zu vermessen. Hinreichende Gerätekapazitäten sind insbesondere bei den eng getakteten initialen Entnahmezeitpunkten wie Nullpunkt, 8 h und 12 h zu planen.
Vielleicht konnten wir Ihnen mit unseren oben angeführten Überlegungen ohne Anspruch auf Vollständigkeit praxisnahe Hinweis geben. Wir freuen uns auf Ihre Einwertungen, Anregungen und Beobachtungen und natürlich auch auf Fragen zur praktischen Durchführung.
1) Den Titel Voll kompatibel? sollten Sie bitte mit Humor sehen: So wie Ihre Zubereitungen steril, nicht etwa: absolut steril sind, müssen Ihre Zubereitungen natürlich nur kompatibel sein.

