Drei einfachere Versuche zum besseren Verständnis der luftgetragenen, molekularen Kontamination
Von Wolfgang Woiwode
Schlüsselwörter: Luftgetragene, molekulare Kontamination, Reinigungsvalidierung, Henry-Gesetz
Key words: Airborne molecular contamination, AMC, Cleaning Validation, Henry´s Law
Mit einem, wie wir meinten, einfachen Versuch hatten wir unsere Experimente zur luftgetragenen, molekularen Kontamination (Airborne molecular contamination, AMC) fortgesetzt: In eine Metallkiste mit den Abmessungen 700 mm x 360 mm x 380 mm (L x B x H) und einem Gesamtvolumen von rund 97 Litern, unserer „Mottenkiste“, hatten wir einzeln in Bechergläsern jeweils 50 mL Wasser, Alkohol, Hexan und Toluol eingebracht. Ziel dieses Versuchs war der nach dem Henry-Gesetz erwartungsgemäße Nachweis der wechselweisen Durchdringung dieser vier Verbindungen über die Umgebungsluft im abgeschlossenen System. Mit Verwendung von Bechergläsern mit unterschiedlichen Durchmessern für das Wasser wollten wir auch gleich Hinweise auf die Kinetik des luftgetragenen Austauschs gewinnen. Die wechselweisen Übergänge verfolgten wir mittels der Gesamtkohlenstoffbestimmung, UV-Spektralphotometrie und Gaschromatographie. Die Ergebnisse zeigten, dass die genannten Verbindungen hinsichtlich des luftgetragenen, molekularen Austauschs einerseits Donatoren, andererseits aber auch Akzeptoren repräsentieren. Einfacher ausgedrückt: Im Luftkontakt erfolgt wechselweise Kontamination. Die Daten waren jedoch zu komplex, um erste Aussagen zur Kinetik des luftgetragenen Austauschs zu machen. Wir mussten zurückrudern, die Experimente überschaubarer gestalten. Wir entschieden uns für drei vom Design her einfachere Versuche zur luftgetragenen, molekularen Kontamination mit dem binären System Wasser und Alkohol: AMC und Oberfläche, AMC und Zeit, und AMC und Temperatur
AMC und Oberfläche
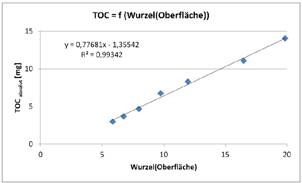
Abbildung 1, AMC und Oberfläche
Versuchsziel: Prüfung der Abhängigkeit des Eintrags von Kohlenstoff aus der Luft in Wasser in Abhängigkeit von der Oberfläche der gleicher Wassermengen bei einem definierten Klima und Normaldruck. In diesem Versuch wurde von der zufälligen Organikfracht der Luft in unserer Klimakammer 30 °C ± 2 °C/65 % RH ± 5 % RH ausgegangen
Durchführung: Sieben Glasschalen mit Durchmessern von 66 mm bis 224 mm und gleicher Randhöhe wurden mit je 100 mL Reinstwasser gefüllt und 2 h auf ein Edelstahlregal in der Klimakammer 30 °C / 65 % RH eingestellt. Die Konvektion im Klimaraum sicherte einen gleichmäßigen Kontakt der Wasseroberflächen mit der Umgebungsluft. Nach 2 h wurde der Gesamtkohlenstoffgehalt des Wassers jeder Glasschale nach Ph. Eur. 2.2.44 Total Organic Carbon (TOC) bestimmt.
Ergebnisse: Es wurde eine Zunahme des Kohlenstoffgehalts des Wassers von der kleinsten bis zur größten Glasschale festgestellt. Es besteht ein linearer Zusammenhang in der Form TOC = f(Wurzel(Oberfläche)) (Abbildung 1).
AMC und Temperatur
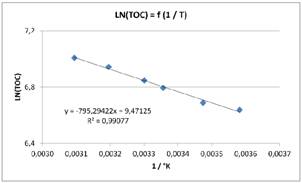
Abbildung 2, AMC und Temperatur
Versuchsziel: Prüfung der Abhängigkeit des luftgetragenen Eintrags von Kohlenstoff in Wasser in Abhängigkeit von der Temperatur am Beispiel des binären Systems Wasser/Ethanol in einem abgeschlossenen Kompartiment.
Durchführung: In sechs V4A-Spanndeckelbehälter mit einem Volumen von je 4 L wurden je 2 Bechergläser mit einem Volumen von je 250 mL eingebracht. In eines der beiden Bechergläser wurden 50 mL Reinwasser, und in das weitere Becherglas 50 mL Ethanol 96 % gegeben. Die Spanndeckel wurden aufgesetzt und verschlossen. Je ein Behälter wurde über 4 h bei 5 °C, 25 °C, 30 °C, 40 °C und 50 °C belassen. Danach wurden die Behälter auf Raumtemperatur gebracht, und der Inhalt des Becherglases, in dem Wasser vorgelegt wurde, nach Ph. Eur. 2.2.44 auf Gesamtkohlenstoff untersucht.
Ergebnisse: Der TOC-Gehalt im Wasser steigt durch den luftgetragenen Übergang von Ethanol aus dem anderen Becherglas mit der Temperatur von 5 °C bis zur gemessenen, maximalen Temperatur 50 °C an. Es besteht ein linearer Zusammenhang in der Form ln(TOC)=f(1/T) (Abbildung 2).
AMC und Zeit
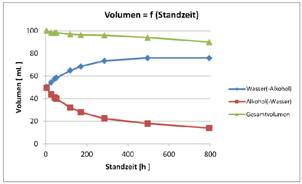
Abbildung 3, AMC und Zeit
Versuchsziel: Prüfung des luftgetragenen Übergangs von Ethanol in Wasser und von Wasser in Ethanol in Abhängigkeit von der Zeit am Beispiel des binären Systems Wasser/Ethanol in einem abgeschlossenen Kompartiment.
Durchführung: In sieben V4A-Spanndeckelbehälter mit einem Volumen von 4 L wurden je 2 Bechergläser mit einem Volumen von je 250 mL eingebracht (Abbildung). In eines der beiden Bechergläser wurden 50 mL Reinwasser, und in das weitere Becherglas 50 mL Ethanol 96 % gegeben. Die Spanndeckel wurden aufgesetzt und verschlossen. Die Behälter wurden bei 30 °C ± 2 °C in eine unserer Klimakammern eingestellt. Über einen Zeitraum von 33 Tagen wurde jeweils ein Behälter entnommen und auf Raumtemperatur gebracht. Aus den vorausgegangenen Experimenten war bereits bekannt, dass nach entsprechender Standzeit Gemische von Wasser und Alkohol vorliegen. Untersucht wurden daher im Fall beider Bechergläser das Volumen, die Dichte, der Brechungsindex und der TOC-Gehalt der Lösungen.
Ergebnisse: Im dem abgeschlossenen Kompartiment nahm das Volumen der Lösung im ursprünglichen Wasserbecherglas anfangs schnell, dann stetig zu. Umgekehrt nahm das Volumen der Lösung im ursprünglichen Alkoholbecherglas stetig ab. Im Fall beider Bechergläser wurde nach 30 Tagen die gleiche Mischung Wasser/Alkohol gefunden, was den wechselweisen Übergang von Wasser und Alkohol einerseits bestätigte, andererseits aber schließlich im Gleichgewicht befindlich offensichtlich beendete. Gleichzeitig nahm die Kondens-Wasser-Alkohol-Bildung an den Innenwänden des V4A-Behälters zu, was das in beiden Bechergläsern gemessene Gesamtvolumen dementsprechend verringerte (Abbildung 3).
Findungen
Mit dem Versuch AMC und Oberfläche wurde belegt, dass der luftgetragene Eintrag kohlenstoffhaltiger Verbindungen proportional zur steigenden Wasseroberfläche verläuft. Der lineare Bezug TOC = f(Wurzel(Oberfläche)) unter den gewählten Bedingungen kann zufällig sein, und sollte nicht zur Berechnung von Stoffübergängen über große Wasseroberflächen herangezogen werden. Abgeschätzt werden kann aber in jedem Fall, dass die Masseübergänge aus der Luft in Abhängigkeit von der Wasseroberfläche z.B. von Seen und der Zeit im Bereich von g und kg sehr groß sind.
Aus dem Versuch AMC und Temperatur geht hervor, dass die treibende Kraft für den Phasenübergang in das Wasser nach dem Henry-Gesetz der Partialdruck des gasförmigen Luftinhaltsstoffs ist. Da der Partialdruck mit der Temperatur einerseits ansteigt, andererseits die Stoffkonzentrationen im Wasser aber zunächst weit unterhalb der Sättigungsgrenze liegt, steigt der Stoffübergang in das Wasser mit der Temperatur.
Der Versuch AMC und Zeit schließlich zeigt, dass in Abhängigkeit vom Partialdruck über die Zeit erhebliche Massetransporte ablaufen: Ethanol ist in unserem Beispiel mit einem Übergang von mehr als 40 mL in das Wasser hinein ganz einfach schneller. Wasser mit niedrigerem Dampfduck diffundiert in gleicher Weise in das Becherglas, in dem ursprünglich Ethanol vorgelegt wurde. Der wechselweise Übergang endet bei Wasser/Alkohol-Gemischen gleicher Konzentration, wobei die im Gleichgewicht befindlichen Lösungen unterschiedlichen Volumens jetzt auch die V4A-Wandungen mit Kondensbildung beaufschlagen. Wir sehen dies als Beweis, dass Wasser hinsichtlich der Aufnahme von Ethanol zunächst als Schwamm wirkt. Nach Sättigung beginnt dann jedoch die Kontamination der Behälterinnenwand, da deren Temperatur unter den Siedepunkten von Wasser und Ethanol liegt.
Relevanz für die Reinigungsvalidierung
Grundlagenforschung ist unabdingbar und häufig sehr interessant. Wie ist jedoch die Relevanz dieser Findungen für die Reinigungsvalidierung? Aus unserer Sicht wie folgt:
Die beschriebenen Stofftransporte durch die Luft laufen immer ab, wenn Wirkstoffe, Hilfsstoffe, Reinigungsmittel, Wasser, Lösungsmittel und Kontaminanten sublimieren oder verdampfen und können als Systeme von Donatoren und Akzeptoren beschrieben werden.
Das Ausmaß der Stofftransporte steigt proportional zur Oberfläche der beteiligten Stoffe und Medien, häufig Wasser.
Das Ausmaß der Stofftransporte steigt proportional mit der Temperatur.
Volumenveränderungen, Änderung z.B. von Brechungsindizes und Dichten, messtechnisch nachweisbare und organoleptisch wahrnehmbare Kontamination können unerwünschte Folgen des luftgetragenen, molekularen Austauschs sein. Die Überlegungen sollten in der Herstellung von Arzneimitteln berücksichtigt werden, und in jedem Fall Eingang in die Festlegungen der Akzeptanzkriterien in der Reinigungsvalidierung finden.

